Giáo án Hóa học Khối 8 - Tuần 13 - Năm học 2017-2018 - Trường THCS Ngô Quang Nhã
I.MỤC TIÊU:
1. Kiến thức
- Củng cố lại các kiến thức ở chương II.
- Vận dụng thành thạo các dạng bài tập:
+ Lập công thức hóa học và lập phương trình hóa học.
+ Biết vận dụng ĐL BTKL vào giải các bài toán hóa học đơn giản.
+ Xác định nguyên tố hóa học.
2. Kĩ năng: Tư duy và trình bày
3. Thái độ: Giáo dục cho HS ý thức nghiêm túc làm bài.
II. CHUẨN BỊ:
1. Giáo viên : Ma trận + đề + đáp
Đề kiểm tra 1 tiết (hệ thống câu hỏi trắc nghiệm + bài tập tự luận)
2. Học sinh: Ôn tập kiến thức ở chương II.
III. CÁC BƯỚC LÊN LỚP:
- Ổn định lớp:
- Kiểm tra bài cũ: (Không)
- Nội dung kiểm tra:
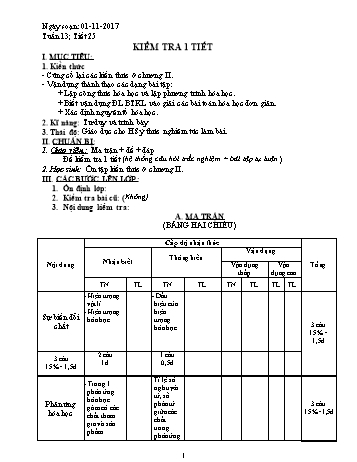
- MA TRẬN
(BẢNG HAI CHIỀU)
Bạn đang xem tài liệu "Giáo án Hóa học Khối 8 - Tuần 13 - Năm học 2017-2018 - Trường THCS Ngô Quang Nhã", để tải tài liệu gốc về máy hãy click vào nút Download ở trên.
Tóm tắt nội dung tài liệu: Giáo án Hóa học Khối 8 - Tuần 13 - Năm học 2017-2018 - Trường THCS Ngô Quang Nhã
Ngày soạn: 01-11-2017 Tuần 13; Tiết 25 KIỂM TRA 1 TIẾT I. MỤC TIÊU: 1. Kiến thức - Củng cố lại các kiến thức ở chương II. - Vận dụng thành thạo các dạng bài tập: + Lập công thức hóa học và lập phương trình hóa học. + Biết vận dụng ĐL BTKL vào giải các bài toán hóa học đơn giản. + Xác định nguyên tố hóa học. 2. Kĩ năng: Tư duy và trình bày 3. Thái độ: Giáo dục cho HS ý thức nghiêm túc làm bài. II. CHUẨN BỊ: 1. Giáo viên : Ma trận + đề + đáp Đề kiểm tra 1 tiết (hệ thống câu hỏi trắc nghiệm + bài tập tự luận) 2. Học sinh: Ôn tập kiến thức ở chương II. III. CÁC BƯỚC LÊN LỚP: Ổn định lớp: Kiểm tra bài cũ: (Không) Nội dung kiểm tra: MA TRẬN (BẢNG HAI CHIỀU) Nội dung Cấp độ nhận thức Tổng Nhận biết Thông hiểu Vận dụng Vận dụng thấp Vận dụng cao TN TL TN TL TN TL TL TL Sự biến đổi chất - Hiện tượng vật lí. - Hiện tượng hóa học - Dấu hiệu của hiện tượng hóa học 3 câu 15% = 1,5đ 3 câu 15%= 1,5đ 2 câu 1đ 1 câu 0,5đ Phản ứng hóa học - Trong 1 phản ứng hóa học gòm có các chất tham gia và sản phẩm Tỉ lệ số nghuyên tử, số phân tử giữa các chất trong phản ứng 3 câu 15%=1,5đ 3 câu 15%= 1,5đ 2 câu 1đ 1 câu 0,5đ Định luật bảo toàn khối lượng - Áp dụng định luật - Lập PTHH - Áp dụng ĐLBTKL 2 câu 35%= 3,5đ 2 câu 35%= 3,5đ 1 câu 0,5đ 1 câu 3đ Phương trình hóa học PTHH - Ý nghĩa của PTHH - Lập PTHH 3 câu 35%= 3,5đ 3 câu 35%= 3,5đ 1 câu 1đ 1 câu 0,5đ 1 câu 2đ Tổng số câu 11 Tổng số điểm 10 Tỉ lệ 100% 6 câu 3,5đ 35% 4câu 3,5đ 35% 1 câu 3đ 30% Tổng số câu 11 Tổng số điểm 10 Tỉ lệ 100% B. ĐỀ: ĐỀ: 1 I. Phần trắc nghiệm: (4đ) * Khoanh tròn vào chữ cái đầu mỗi câu mà em cho là đúng nhất: Câu 1: Đâu là hiện tượng hóa học trong các hiện tượng dưới đây? A. Nước sôi B. Nước bốc hơi C. Nước bị phân hủy tạo thành khí oxi và khí hidro D. Nước đóng băng Câu 2: Đâu là hiện tượng vật lí trong các hiện tượng dưới đây? A. Dây sắt cắt nhỏ từng đoạn và tán thành đinh sắt B. Đường cháy thành than C. Nước phân hủy thành hiđrô và nước D. Dao bằng sắt lâu ngày bị gỉ Câu 3: Làm thế nào để biết có phản ứng xảy ra? A. Dựa vào mùi của sản phẩm B. Dựa vào màu của sản phẩm C. Dựa vào sự tỏa nhiệt D. Dựa vào dấu hiệu có chất mới tạo thành Câu 4: Trong phản ứng sau chất nào là chất tham gia? Axit clohidric + Natri cacbonat à Natriclorua + Cacbon đioxit + Nước A. Axit clohidric, Natriclorua B. Natriclorua, Cacbon đioxit, C. Axit clohidric, Natricacbonat D. Natriclorua, Cacbonđioxit, Nước Câu 5: Trong phản ứng sau chất nào là chất sản phẩm? Axit clohidric + Natri cacbonat à Natriclorua + Cacbonđioxit + Nước A. Axit clohidric, Natriclorua B. Natriclorua, Cacbon đioxit, B. Cacbob đioxit, Nước D. Natriclorua, Cacbonđioxit, Nước Câu 6: Cho phản ứng hóa học sau: Zn + 2HCl ZnCl2 + H2 Cho biết chất tham gia: Zn tác dụng với HCl có tỉ lệ là: A. 1 : 2 B. 1 : 1 C. 2 : 1 D. 2 : 2. Câu 7: Cho 4 gam khí Cacbon tác dụng hết 12 gam khí ôxi tạo thành bao nhiêu gam khí Cacbonic? A. 12 gam B. 16 gam C. 18 gam D. 36 gam. Câu 8: Cho PTHH: 4Na + ? → 2Na2O Chất cần điền vào dấu chấm hỏi là: A. O B. O2 C. 2O D. Na II. Phần tự luận: (6đ) Câu 9: (1 điểm) Phương trình hóa học biểu diễn gì, gồm công thức hóa học của những chất nào? Câu 10: (2 điểm) Lập phương trình phản ứng hóa học theo sơ đồ sau: a. P + O2 ----> P2O5 b. SO2 + O2 ----> SO3 Câu 11: (3 điểm) Cho 24 g kim loại Magie (Mg) tác dụng với axít Clohiđric (HCl) thu được 46g muối Magieclorua (MgCl2) và 2g khí Hiđro (H2) a. Lập phương trình hóa học của phản ứng? b. Tính khối lượng axit clohđric đã dùng? ĐỀ: 2 I. Phần trắc nghiệm: (4đ) * Khoanh tròn vào chữ cái đầu mỗi câu mà em cho là đúng nhất: Câu 1: Trong phản ứng sau chất nào là chất tham gia? Axit clohidric + Natri cacbonat à Natriclorua + Cacbon đioxit + Nước A. Axit clohidric, Natriclorua B. Natriclorua, Cacbon đioxit, C. Axit clohidric, Natricacbonat D. Natriclorua, Cacbonđioxit, Nước Câu 2: Đâu là hiện tượng vật lí trong các hiện tượng dưới đây? A. Dây sắt cắt nhỏ từng đoạn và tán thành đinh sắt B. Đường cháy thành than C. Nước phân hủy thành hiđrô và nước D. Dao bằng sắt lâu ngày bị gỉ Câu 3: Làm thế nào để biết có phản ứng xảy ra? A. Dựa vào mùi của sản phẩm B. Dựa vào màu của sản phẩm C. Dựa vào sự tỏa nhiệt D. Dựa vào dấu hiệu có chất mới tạo thành Câu 4: Đâu là hiện tượng hóa học trong các hiện tượng dưới đây? A. Nước sôi B. Nước bốc hơi C. Nước đóng băng D. Nước bị phân hủy tạo thành khí oxi và khí hidro Câu 5: Cho PTHH: 4Na + ? → 2Na2O Chất cần điền vào dấu chấm hỏi là: A. O B. O2 C. 2O D. Na Câu 6: Cho phản ứng hóa học sau: Zn + 2HCl ZnCl2 + H2 Cho biết chất tham gia: Zn tác dụng với HCl có tỉ lệ là: A. 1 : 1 B. 1 : 2 C. 2 : 1 D. 2 : 2. Câu 7: Cho 4 gam khí Cacbon tác dụng hết 12 gam khí ôxi tạo thành bao nhiêu gam khí Cacbonic? A. 12 gam B. 18 gam C. 16 gam D. 36 gam. Câu 8: Trong phản ứng sau chất nào là chất sản phẩm? Axit clohidric + Natri cacbonat à Natriclorua + Cacbonđioxit + Nước A. Natriclorua, Cacbonđioxit, Nước B. Natriclorua, Cacbon đioxit, B. Cacbob đioxit, Nước D. Axit clohidric, Natriclorua II. Phần tự luận: (6đ) Câu 9: (1 điểm) Phương trình hóa học biểu diễn gì, gồm công thức hóa học của những chất nào? Câu 10: (2 điểm) Lập phương trình phản ứng hóa học theo sơ đồ sau: a. P + O2 ----> P2O5 b. SO2 + O2 ----> SO3 Câu 11: (3 điểm) Cho 24 g kim loại Magie (Mg) tác dụng với axít Clohiđric (HCl) thu được 46g muối Magieclorua (MgCl2) và 2g khí Hiđro (H2) a. Lập phương trình hóa học của phản ứng? b. Tính khối lượng axit clohđric đã dùng? ĐỀ: 3 I. Phần trắc nghiệm: (4đ) * Khoanh tròn vào chữ cái đầu mỗi câu mà em cho là đúng nhất: Câu 1: Làm thế nào để biết có phản ứng xảy ra? A. Dựa vào mùi của sản phẩm B. Dựa vào màu của sản phẩm C. Dựa vào sự tỏa nhiệt D. Dựa vào dấu hiệu có chất mới tạo thành Câu 2: Đâu là hiện tượng vật lí trong các hiện tượng dưới đây? A. Dao bằng sắt lâu ngày bị gỉ B. Đường cháy thành than C. Nước phân hủy thành hiđrô và nước D. Dây sắt cắt nhỏ từng đoạn và tán thành đinh sắt Câu 3: Đâu là hiện tượng hóa học trong các hiện tượng dưới đây? A. Nước bị phân hủy tạo thành khí oxi và khí hidro B. Nước bốc hơi C. Nước đóng băng D. Nước sôi Câu 4: Trong phản ứng sau chất nào là chất tham gia? Axit clohidric + Natri cacbonat à Natriclorua + Cacbon đioxit + Nước A. Axit clohidric, Natriclorua B. Natriclorua, Cacbon đioxit, C. Axit clohidric, Natricacbonat D. Natriclorua, Cacbonđioxit, Nước Câu 5: Trong phản ứng sau chất nào là chất sản phẩm? Axit clohidric + Natri cacbonat à Natriclorua + Cacbonđioxit + Nước A. Axit clohidric, Natriclorua B. Natriclorua, Cacbon đioxit, C. Natriclorua, Cacbonđioxit, Nước D. Cacbon đioxit, Nước Câu 6: Cho PTHH: 4Na + ? → 2Na2O Chất cần điền vào dấu chấm hỏi là: A. O B. O2 C. 2O D. Na Câu 7: Cho 4 gam khí Cacbon tác dụng hết 12 gam khí ôxi tạo thành bao nhiêu gam khí Cacbonic? A. 12 gam B. 16 gam C. 18 gam D. 36 gam. Câu 8: Cho phản ứng hóa học sau: Zn + 2HCl ZnCl2 + H2 Cho biết chất tham gia: Zn tác dụng với HCl có tỉ lệ là: A. 1 : 2 B. 1 : 1 C. 2 : 1 D. 2 : 2. II. Phần tự luận: (6đ) Câu 9: (1 điểm) Phương trình hóa học biểu diễn gì, gồm công thức hóa học của những chất nào? Câu 10: (2 điểm) Lập phương trình phản ứng hóa học theo sơ đồ sau: a. P + O2 ----> P2O5 b. SO2 + O2 ----> SO3 Câu 11: (3 điểm) Cho 24 g kim loại Magie (Mg) tác dụng với axít Clohiđric (HCl) thu được 46g muối Magieclorua (MgCl2) và 2g khí Hiđro (H2) a. Lập phương trình hóa học của phản ứng? b. Tính khối lượng axit clohđric đã dùng? ĐỀ: 4 I. Phần Trắc nghiệm: (4đ) * Khoanh tròn vào chữ cái đầu mỗi câu mà em cho là đúng nhất: Câu 1: Trong phản ứng sau chất nào là chất sản phẩm? Axit clohidric + Natri cacbonat à Natriclorua + Cacbonđioxit + Nước A. Axit clohidric, Natriclorua B. Natriclorua, Cacbon đioxit, B. Cacbob đioxit, Nước D. Natriclorua, Cacbonđioxit, Nước Câu 2: Đâu là hiện tượng vật lí trong các hiện tượng dưới đây? A. Dây sắt cắt nhỏ từng đoạn và tán thành đinh sắt B. Đường cháy thành than C. Nước phân hủy thành hiđrô và nước D. Dao bằng sắt lâu ngày bị gỉ Câu 3: Làm thế nào để biết có phản ứng xảy ra? A. Dựa vào mùi của sản phẩm B. Dựa vào màu của sản phẩm C. Dựa vào sự tỏa nhiệt D. Dựa vào dấu hiệu có chất mới tạo thành Câu 4: Trong phản ứng sau chất nào là chất tham gia? Axit clohidric + Natri cacbonat à Natriclorua + Cacbon đioxit + Nước A. Axit clohidric, Natriclorua B. Natriclorua, Cacbon đioxit, C. Axit clohidric, Natricacbonat D. Natriclorua, Cacbonđioxit, Nước Câu 5: Đâu là hiện tượng hóa học trong các hiện tượng dưới đây? A. Nước sôi B. Nước bốc hơi C. Nước đóng băng D. Nước bị phân hủy tạo thành khí oxi và khí hidro Câu 6: Cho PTHH: 4Na + ? → 2Na2O Chất cần điền vào dấu chấm hỏi là: A. O B. 2O C. O2 D. Na Câu 7: Cho phản ứng hóa học sau: Zn + 2HCl ZnCl2 + H2 Cho biết chất tham gia: Zn tác dụng với HCl có tỉ lệ là: A. 1 : 1 B. 1 : 2 C. 2 : 1 D. 2 : 2. Câu 8: Cho 4 gam khí Cacbon tác dụng hết 12 gam khí ôxi tạo thành bao nhiêu gam khí Cacbonic? A. 12 gam B. 16 gam C. 18 gam D. 36 gam. II. Phần tự luận: (6đ) Câu 9: (1 điểm) Phương trình hóa học biểu diễn gì, gồm công thức hóa học của những chất nào? Câu 10: (2 điểm) Lập phương trình phản ứng hóa học theo sơ đồ sau: a. P + O2 ----> P2O5 b. SO2 + O2 ----> SO3 Câu 11: (3 điểm) Cho 24 g kim loại Magie (Mg) tác dụng với axít Clohiđric (HCl) thu được 46g muối Magieclorua (MgCl2) và 2g khí Hiđro (H2) a. Lập phương trình hóa học của phản ứng? b. Tính khối lượng axit clohđric đã dùng? C. ĐÁP ÁN: I. Phần Trắc nghiệm: (4đ) Câu 1 2 3 4 5 6 7 8 Đề 1 C A D C D A B B Đề 2 C A D D B B C A Đề 3 D D A C C B B A Đề 4 D A D C D C B B II. Phần tự luận: (6đ) Câu Nội dung Điểm 1 - Phương trình hóa học dùng để biểu diễn ngắn gọn phản ứng hóa học. - Gồm công thức hóa học của những chất tham gia và sản phâm 0.5đ 0.5đ 2 Cân bằng các phương trình hóa học: a. 4P + 5O2 ® 2 P2O5 b. 2SO2 + O2 ® 2SO3 1.0đ 1.0đ 3 a. PTPƯ: Mg + 2HCl g MgCl2 + H2 b. Theo ĐL BTKL: m Mg + m HCl = m MgCl + g m HCl = m MgCl + - m Zn = 46 + 2 – 24 = 24g Vậy khối lượng HCl đã dùng hết là : 24 (g) 1.0đ 0.5đ 0.5đ 0.5đ 0.5đ Bảng thống kê điểm kiểm tra Lớp / sĩ số Thang điểm So sánh lần kiểm tra trước ( từ 5 trở lên) [0 ;5 ) [5 ; 7) [7 ; 9) [9 ; 10) Tăng % Giảm % 8A: 8C: Tổng cộng: IV. RÚT KINH NGHIỆM: GV: HS:. Ngày soạn: 01-11-2017 Tuần 13;Tiết 26 Chương III: MOL VÀ TÍNH TOÁN HÓA HỌC Bài 18: MOL I. MỤC TIÊU: 1. Kiến thức - Ý nghĩa của mol, khối lượng mol, thể tích mol - Định nghĩa: mol, khối lượng mol, thể tích mol của chất khí ở điều kiện tiêu chuẩn (đktc): (0oC, 1 atm). - Biểu thức biểu diễn mối liên hệ giữa lượng chất (n), khối lượng (m) và thể tích (V). 2. Kĩ năng - Tính được khối lượng mol nguyên tử, mol phân tử của các chất theo công thức. - Kĩ năng tính phân tử khối. 3.Thái độ - Tạo hứng thú cho học sinh yêu thích môn học II. CHUẨN BỊ: 1. Giáo viên : Hình vẽ 3.1 SGK/ 64 2. Học sinh: Đọc SGK / 63,64 III. CÁC BƯỚC LÊN LỚP: 1. Ổn định lớp: (1/) 2. Kiểm tra bài cũ: (Không) 3. Bài mới GV đặc câu hỏi để vào bài mới: Các em có biết mol là gì không ?. Để biết mol là gì tiết học này các em sẽ tìm hiểu. Hoạt động của giáo viên Hoạt động của học sinh Nội dung Hoạt động 1: Tìm hiểu mol là gì (14/) - Mol là lượng chất có chứa 6.1023 nguyên tử hay phân tử của chất đó. - 6.1023 được làm tròn từ số 6,02204.1023 và được gọi là số Avôgađro kí hiệu là N. - Trong 1 mol nguyên tử Fe có chứa bao nhiêu nguyên tử Fe ? -Trong 1 mol phân tử H2O chứa bao nhiêu phân tử H2O ? Vậy, theo em các chất có số mol bằng nhau thì số nguyên tử (phân tử) sẽ như thế nào ? - Nếu nói: “1 mol Hiđro”, em hiểu câu nói này như thế nào ? Vậy để tránh sự nhầm lẫn đó, ta phải nói như thế nào ? - Yêu cầu HS làm bài tập 1 SGK/ 65 - Yêu cầu HS các nhóm trình bày, bổ sung. - Đưa ra đáp án, yêu cầu HS nhận xét. - Nghe và ghi nhớ : - HS đọc mục “em có biết” - 1 mol nguyên tử Fe chứa 6.1023 ( hay N) nguyên tử Fe. - 1 mol phân tử H2O chứa 6.1023 ( hay N) phân tử H2O. - Các chất có số mol bằng nhau thì số nguyên tử (phân tử) sẽ bằng nhau. -“1 mol Hiđro”, nghĩa là: + 1 mol nguyên tử Hiđro. + Hay 1 mol phân tử Hiđro. - Thảo luận nhóm (5’) để làm bài tập 1: a. Cứ 1 mol Al - 6.1023 nguyên tử vậy 1,5 mol - x nguyên tử g Vậy trong 1,5 mol nguyên tử Al có chứa 9.1023 nguyên tử Al. b.3.1023 phân tử H2 c.1,5.1023 phân tử NaCl. d.0,3.1023 phân tử H2O. I. Mol là gì ? - Mol là lượng chất có chứa N (6.1023) nguyên tử hay phân tử của chất đó. Hoạt động 2: Tìm hiểu khối lượng Mol (10/) - Giới thiệu: Khối lượng mol (M) là khối lượng của 1 chất tính bằng gam của N nguyên tử hay phân tử chất đó. - Giáo viên đưa ra khối lượng mol của các chất: Al, O2, CO2, H2O, N2. g yêu cầu HS nhận xét về khối lượng mol và NTK hay PTK của chất ? - Bài tập: Tính khối lượng mol của: H2SO4, SO2, CuO, C6H12O6. - Gọi 4 HS lên làm bài tập. - Nhận xét, đưa ra kết quả đúng. - Nghe và ghi nhớ. - HS tính nguyên tư-phân tử khối của: Al, O2, CO2, H2O, N2. 27, 32, 44 , 18 ,28 - Khối lượng mol và NTK (PTK) có cùng số trị nhưng khác đơn vị. - Thảo luận nhóm giải bài tập: + Khối lượng mol H2SO4 = 98g + Khối lượng mol SO2 = 64g + Khối lượng mol CuO = 76g + Khối lượng mol C6H12O6 = 108g II. Khối lượng Mol là gì ? - Khối lượng mol (kí hiệu là M) của 1 chất là khối lượng tính bằng gam của N nguyên tử hay phân tử chất đó. - Thí dụ: (sgk) Hoạt động 3: Tìm hiểu thể tích Mol của chất khí (12/) - Yêu cầu HS nhắc lại khối lượng mol g Em hiểu thể tích mol chất khí là gì ? - Yêu cầu HS quan sát hình 3.1 SGK/ 64 + Trong cùng điều kiện: t0, p thì khối lượng mol của chúng như thế nào ? + Em có nhận xét gì về thể tích mol của chúng ? Vậy trong cùng điều kiện: t0, p thì 1 mol của bất kì chất khí nào cũng đều chiếm thể tích bằng nhau. Và ở điều kiện tiêu chuẩn (t0=0, p =1 atm) thì V của các chất khí đều bằng nhau và bằng 22,4 lít. - Thể tích mol của chất khí là thể tích chiếm bởi N phân tử 3 chất khí đó. - Quan sát hình vẽ và trả lời câu hỏi : + Trong cùng điều kiện: t0, p thì khối lượng mol của chúng khác nhau. Còn thể tích mol của chúng lại bằng nhau. - Nghe và ghi nhớ: Ở đktc, 1 mol chất khí có V khí = 22,4 lít. III. Thể tích mol của chất khí là gì ? - Thể tích mol của chất khí là thể tích chiếm bởi N phân tử chất đó. - Ở đktc (00C, 1atm) thì thể tích mol của các chất khí đều bằng 22,4 lít. 4. Củng cố: (5/) Bài tập: Nếu em có 1 mol phân tử H2 và 1 mol phân tử O2 , hãy cho biết: a. Số phân tử mỗi chất là bao nhiêu ? b. Khối lượng mol của mỗi chất là bao nhiêu ? c. Thể tích mol của các khí trên khi ở cùng điều kiện t0, p là thế nào ? Nếu ở cùng đktc, chúng có thể tích là bao nhiêu ? 5. Hướng dẫn HS tự học, làm bài tập và soạn bài mới ở nhà: (3 phút) - Học bài. - Làm bài tập 1c,d, 2, 3b SGK/65 - Đọc bài 19 SGK/66 IV. RÚT KINH NGHIỆM: GV:...................... HS:. Châu Thới, ngày tháng 11 năm 2017 Kí duyệt
File đính kèm:
 giao_an_hoa_hoc_khoi_8_tuan_13_nam_hoc_2017_2018_truong_thcs.doc
giao_an_hoa_hoc_khoi_8_tuan_13_nam_hoc_2017_2018_truong_thcs.doc

